Coagulopatía asociada a COVID-19
26/03/2021
Los casos severos de COVID-19 desarrollan un Síndrome de Respuesta Inflamatoria Sistémico, así como un Síndrome Respiratorio Agudo Severo en el cual se implican, además de los cambios inflamatorios, alteraciones del endotelio vascular pulmonar y desarrollo de microtrombos
En diciembre de 2019, surgió en la ciudad de Wuhan, China, una nueva enfermedad infecciosa con alta capacidad de contagio. Se diseminó rápidamente en todo el mundo y se declaró como pandemia en marzo de 2020. El agente causante de esta nueva patología conocida como COVID-19 (Coronavirus Disease-2019) se identificó como un nuevo coronavirus, denominado SARS-CoV-2 (Severe Acute Respiratory Syndrome Coronavirus 2).
Las investigaciones orientan hacia que la proteína S de la superficie viral se une a la enzima convertidora de angiotensina 2 (ACE2) (responsable del paso de angiotensina II a angiotensina III), expresada en las células del epitelio respiratorio, desencadenando mecanismos que conllevan al ingreso del virus a la célula, donde logra generar su replicación, al igual que desencadenar diversos tipos de respuesta biológica. Se sabe que el grupo de virus al cual pertenece el SARS-CoV-2 genera una regulación a la baja de la ACE2 que resulta en un incremento de la angiotensina II (AT-II). La gravedad del cuadro de COVID-19 se ha visto asociada con edad avanzada y con comorbilidades como Enfermedad Pulmonar Obstructiva Crónica (EPOC), insuficiencia cardíaca, hipertensión arterial (HTA), diabetes mellitus y tabaquismo, condiciones en las que, interesantemente, hay una sobreexpresión de ACE2 en los tejidos pulmonar y cardiaco (Lancet. March 28, 2020).
Los casos severos de COVID-19 desarrollan un Síndrome de Respuesta Inflamatoria Sistémico (SIRS), motivo de revisiones anteriores en este boletín, así como un Síndrome Respiratorio Agudo Severo (SARS) en el cual se implican, además de los cambios inflamatorios, alteraciones del endotelio vascular pulmonar y desarrollo de microtrombos como parte de una coagulopatía llamada “coagulopatía asociada a COVID-19”.
Conceptos sobre hemostasia a tener en cuenta para comprender la coagulopatía asociada a COVID-19
El sistema hemostático tiene como función primordial evitar la pérdida de sangre desde los vasos sanguíneos, y sus componentes más importantes están en el endotelio vascular, las plaquetas y diversas proteínas plasmáticas llamadas “factores de la coagulación”.
Una vez se produce una herida se inicia un proceso para detener la hemorragia, denominado hemostasia primaria, en el cual las mayores protagonistas son las plaquetas, las cuales desencadenan fenómenos de adherencia a proteínas de la matriz extracelular expuestas, así como de liberación de gránulos y agregación entre ellas, formando así un trombo en pocos segundos. Posteriormente se inicia la “hemostasia secundaria”, en la cual intervienen los factores de la coagulación que finalizan con la formación de fibrina. Ambos eventos están estrechamente relacionados y autorregulados.
Las plaquetas se adhieren al colágeno del subendotelio vascular a través de receptores como la glucoproteína (Gp) IaIIa (α2β1) o el FcγRIIA. También se unen a través de una molécula estabilizadora intermediaria, el factor de von Willebrand. Posteriormente las plaquetas se agregan entre sí uniéndose con el fibrinógeno a través de su receptor Gp IIbIIIa (αIIbβ3 o CD41/CD61) (Figura 1).
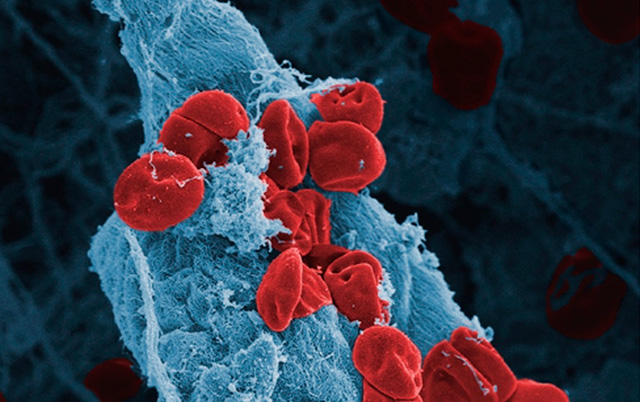
Figura 1. Imagen de microscopia electrónica que ilustra la ruptura de un vaso, donde se presentan los fenómenos plaquetarios de adhesión (unión al colágeno subendotelial) y agregación (unión entre sí). Las integrinas implicadas en estos dos procesos son la α2β1 en el primero y αIIbβ3 en el segundo. La Gp IV y el factor de Von Willebrand son fundamentales en el proceso de adhesión (Cortesía Wellcome Collection).
Una vez se altera el endotelio vascular y las plaquetas empiezan a ejercer sus acciones de adhesión y agregación, paralelamente se activa la llamada hemostasia secundaria, en donde las proteínas plasmáticas de la vía intrínseca de la coagulación (XII, IX, VIII, X, V, entre otros) se activan en cadena para llegar finalmente al paso de la protrombina a trombina, que convierte el fibrinógeno en fibrina, la cual se estabiliza con el factor XIII. De otra parte, en diversos procesos biológicos, como ciertas infecciones (donde se incluyen virus), se incrementa la expresión del factor tisular a nivel endotelial, el cual se une al factor VII formando un complejo que a su vez activa los factores IX y X, desencadenándose la formación de trombina y así confluyendo en los mismos procesos de la vía intrínseca. Esta última es llamada vía extrínseca de la coagulación. La fibrina, por acción de la plasmina, se puede degradar y generar productos como el dímero D (Figura 2).
Figura 2. Cascada de la coagulación con sus dos vías, intrínseca y extrínseca. Se presentan además los sistemas reguladores más importantes y el proceso fibrinolítico.
Procesos patológicos conocidos hasta el momento sobre coagulopatía asociada a COVID-19
Muchos de los pacientes con enfermedad severa desarrollan una coagulopatía trombótica (J Thromb Thrombolysis. May 15, 2020), manifestada clínicamente como trombosis venosa profunda de miembros inferiores, accidentes cerebrovasculares, acroisquemia (Zhonghua Xue Ye Xue Za Zhi. March 28, 2020) y en forma muy prevalente (hasta 27% de los casos) presencia de trombos en el lecho pulmonar como consecuencia probable de tromboembolismo (Eur Heart J. May 14, 2020) o de generación de trombos in situ en la microcirculación pulmonar (Thromb Res. July, 2020).
En los estudios de autopsias se encuentran, fuera de un edema difuso del parénquima, trombos de fibrina pequeños adheridos a capilares alveolares que se encuentran engrosados y, en relación a un infiltrado, de linfocitos y neutrófilos. Hay descamación de neumocitos tipo-2. Así se configura una verdadera endotelitis con una respuesta trombótica microvascular (N Engl J Med 2020 May 21, 2020).
Los valores de laboratorio alterados incluyen prolongación de los tiempos de protrombina (PT) y parcial de tromboplastina (PTT), aumento de los niveles séricos de dímero D, bajos niveles de fibrinógeno y trombocitopenia (J Thromb Haemost. Apr, 2020). Esto denota la activación severa de la coagulación con consumo de sus factores y de las plaquetas. También podemos inferir un fenómeno fibrinolítico.
Interesantemente, para poner las cosas más complejas, en algunos pacientes se han encontrado anticuerpos antifosfolípidos, seguramente en relación con activación de la inmunidad humoral (N Engl J Med. April 8, 2020). Se conoce que estos anticuerpos pueden incrementar la expresión del factor tisular, como se observa en los pacientes con síndrome antifosfolipídico (Thromb Haemost. Dec, 1999).
Está por descartarse el papel de la formación de agregados de factor de von Willegrand, la supresión de proteasas reguladoras como el ADAMTS13 o la desencriptación del factor tisular, como se ha observado en procesos infecciosos similares (Proc Natl Acad Sci USA. Sept, 1990; J Mol Cell Cardiol. July, 2008).
Ninguno de los pacientes experimenta fenómenos trombóticos que cumplan criterios estrictos de coagulación intravascular diseminada.
Tanto una respuesta inflamatoria severa (FASEB. July 1, 1995) como el incremento de la AT-II (Platelets. April 7, 2005), como antes se mencionó, son causas conocidas para la sobreexpresión del factor tisular y la activación de la cascada de la coagulación, evento que ha sido asociado con la patogénesis del COVID-19. El Factor Tisular podría estar implicado directamente en el proceso (J Thromb Thrombolysis. Jun 9, 2020).
Figura 3. Resumen de los mecanismos que potencialmente contribuyen al estado protrombótico identificado en pacientes con COVID-19 severo, destacándose en la imagen el del Factor Tisular. ACE2: Enzima Convertidora de Angiotensina 2. ATII: Angiotensina II. Convención de la Evidencia-color de las flechas: Verde: Fuerte; Amarilla: Altamente probable; Morado: Muy probable.
Desde el punto de vista del tratamiento de la coagulopatía asociada a COVID-19, poco se sabe. Al parecer la anticoagulación podría ser útil y reducir la mortalidad (J Thromb Haemost. March 27, 2020), pero en realidad esto está por demostrase. Se necesita ampliar el conocimiento y derivar según ello la terapéutica futura.
Carlos Alberto Cañas Dávila
Internista Reumatólogo
Fundación Valle del Lili,
Universidad ICESI,
Cali, Colombia.

